COVID-19(新型コロナウイルス)のスパイク蛋白が免疫系を惑わせて宿主を攻撃する可能性があることを示唆しています。
この論文はCOVID-19ウイルスのスパイク蛋白の病原性について考察が述べられていますが、病原性スパイク蛋白によるサイトカインストームなどによって各種症状が惹き起こされているとするものです。
この研究はあくまでCOVID-19、SARS-Covのスパイク蛋白の病原性に調べたものであり、むしろワクチンによって非病原性の抗体を混合させることで重症化を抑えるという内容も書かれています。
しかし、示唆されている内容と、VERSなどに報告されているワクチンによる有害事象は一致しています。mRNAワクチンによって体内で生成されているスパイク蛋白が必ず安全であるかどうか、詳細な研究が望まれます。
註釈・リファレンスが必要な人は問題なく論文を読めるでしょうから、省略します。
ResearchSquare;COVID-19およびSARS-CoVウイルスのスパイク・タンパク質によって誘導される病原性抗体
version.1 投稿日: 2021年6月11日
概要
本研究では,ウイルスフリー・マウス・モデルを用いて,病原性の高いコロナウイルス(COVID-19,SARS-CoVウイルスなど)のスパイク蛋白質に特異的な抗体の病原性の役割を検討した。
本研究では、COVID-19やSARS-CoVなどの病原性の高いコロナウイルスのスパイクタンパク質に特異的な抗体の病原性について、ウイルスフリー・マウスを用いて検討した。我々のデータ
これらの病原性抗体は、抗体依存性自己攻撃(ADAA)のメカニズムにより、宿主の脆弱な細胞を標的として結合することがわかった。
これらの病原性抗体は、ADAA(Antibody Dependent Auto-Attack:抗体依存性自己攻撃)のメカニズムにより、損傷した肺上皮細胞などの宿主の脆弱な細胞や組織を標的として結合し、自己攻撃的な免疫反応を開始し
免疫反応を起こし、ARDS、サイトカインの放出、死亡などの重篤な状態に陥る。さらに、この病原性抗体は、腎臓、脳、心臓などにも炎症や出血を引き起こした。しかも病原抗体は、未成熟な胎児組織と結合し、人工妊娠中絶、産褥期、死産、新生児死亡の原因となる。
妊娠マウスの流産、産褥、死産、新生児死亡などの原因となる。これらの病原性抗体の宿主への結合を阻害することで、新しい臨床的介入が可能となる。
COVID-19のパンデミックに対抗するために、これらの病原性抗体の宿主への結合を阻害することで、新たな臨床的介入を行うことができる。さらに、今回の本研究で検討されたADAAの新しい概念は、病原性の高いインフルエンザ感染症など、他の感染症にも適用できる可能性がある。
インフルエンザなどの他の感染症にも応用できる可能性がある。なお、抗スパイク抗体の大部分は非病原性である。
モノクローナル抗体7種類のうち、有意な病原性を示したのは2種類だけだった。コロナウイルス感染症のパンデミック2019(COVID-19)については、世界の人々の健康と経済に対する大きな脅威である。
COVID-19の感染から1週間後には、臨床症状が重症化し、低酸素血症と呼吸困難が進行して急性呼吸困難症候群(ARDS)に急速に移行する。
17%の患者が急性呼吸窮迫症候群(ARDS)に急速に進行し、そのうち65%の患者が多臓器不全のために悪化し死亡している。
同様の臨床的特徴は他の病原性の高い呼吸器ウイルスに感染した患者でも、同様の臨床的特徴が観察されている。
SARS(重症急性呼吸器症候群)ウイルス(SARS-CoV)や中近東呼吸器症候群(MERS)ウイルス(MERS-CoV)、鳥類のH1N5およびH7N9インフルエンザウイルスなど、他の病原性の高い呼吸器ウイルスに感染した患者にも同様の臨床的特徴が見られる。いくつかのケースでは、ウイルス量は重症化した時点でウイルス量が少ない、または検出されないケースもある。
ウイルスだけではなく、他の死因があったことを示唆している。過剰に反応することが報告されている。免疫反応とそれに伴うサイトカイン・ストームが感染者の死の重要な要因となっていることが報告されているが、何がサイトカインストームを起こしたのか、謎に包まれている。
予想外の発見があった。マウスモデルで、抗インフルエンザ血清を妊娠中のマウスに抗インフルエンザウイルス血清を注射すると炎症を引き起こすという意外な発見をした。そこで、病原性の高いウイルスによって誘導されたある種の抗体は、それ自体が病原性を持つのではないかと考えた。
このように、病原性の高いウイルスによって誘導されたある種の抗体は、宿主の細胞や組織を標的とすることで、それ自体が病原性を持つのではないかと考えた。この仮説を証明するために、抗COVID-19ウイルス抗体を含む抗コロナウイルス抗体の病原性を調べた。調査結果
損傷した肺の上皮細胞に結合した抗COVID-19抗体
SARS-CoV-2(COVID-19)ウイルスおよびSARS-CoVウイルスに特異的な抗体を用いて、ヒト肺上皮細胞株A549との結合性を調べた。テストされた抗体のうち7つはSARS-CoV-2のスパイクに特異的なモノクローナル抗体であった。
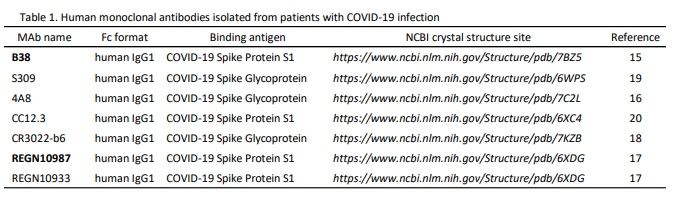
これらの抗体はCOVID-19のB細胞から単離されたもので、他の研究者によって既に報告されている。これら7つのモノクローナル抗体は、その抗体をコードする遺伝子配列に基づいてNCBIの結晶構造サイトから、抗体をコードする遺伝子配列に従って再現した(表1). 試験した他の抗コロナウイルス抗体は以下の通り。
ポリクローナルウサギの抗SARS-CoV-2スパイクワン
(抗COVID-19 S1)、ウサギ抗SARS-CoVスパイク
グリコプロテイン(抗SARS S)、モノクローナルマウス
抗SARS-CoVヌクレオカプシド(N)タンパク質(抗SARS
N). これらの抗体は、市販されている
(Bioss Antibodies社)が市販しているもので、関連する組換え体を動物に免疫して作られた。
SARS-CoV-2およびSARS-CoVウイルスの関連組換えタンパク質で動物を免疫して作製した。
ポリクローナル抗SARS-CoV-2ヌクレオカプシド(N)タンパク質
(ポリクローナル抗体(抗COVID-19 N抗体)は
ポリクローナル抗SARS-CoV-2ヌクレオカプシド(N)蛋白質(抗COVID-19 N)抗体は、組換えのSARS-CoV-2ウイルスのヌクレオカプシド(N)タンパク質をウサギに免疫して得られた(HuaAn McAb Biotechnology)を用いた。
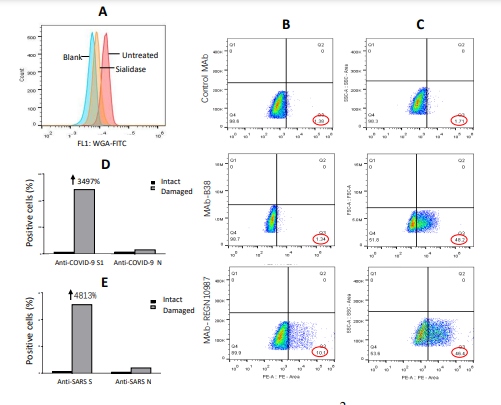
図1. フローサイトメトリーによるヒト肺上皮細胞A549の表面のA549細胞の表面のシアル酸レベルを測定するフローサイトメトリー分析。
健康な細胞(未処理)と損傷を受けた(シアリダーゼ処理)A549細胞、細胞表面のシアル酸が欠損したA549細胞(A)とに特異的な抗体が結合する。
スパイク(S)またはヌクレオキャプシド(N)COVID-19ウイルスやSARSウイルスのスパイクタンパクとSARSウイルスのスパイク(S)またはヌクレオキャプシド(N)タンパク質に特異的な抗体が、健康な(健全なA549細胞(無傷)またはダメージを受けたA549細胞に結合させた(D-E)。B-C:ヒトモノクローナル抗スパイクタンパク質のヒトモノクローナル抗スパイク
抗体B38、REGN10987、およびCR3022-b6(コントロール)健全なA549細胞(B)または損傷を受けたA549細胞(C)に対する損傷を受けたA549細胞への結合を示す。健全な(無傷の)または損傷を受けた肺上皮細胞に対するこれらの抗体の結合は、A549
損傷した肺上皮細胞への結合をA549細胞を用いた。損傷細胞を誘導するために、A549細胞を
ノイラミニダーゼ(シアリダーゼ)で処理した。
メーカーの指示書(Roche社)に従って、ノイラミニダーゼ(シアリダーゼ)で処理した。このとき、蛍光標識したコムギ胚芽アグルチニン(WGA)はN-アセチルノイラミン酸(Vector)に特異的に結合するとフローサイトメトリーによる分析を行い、A549細胞の表面に存在するシアル酸の量を測定した。
細胞表面のシアル酸が欠損した損傷細胞を用いて、生体内の感染した肺上皮の状態を再現した。
感染した肺上皮細胞(シックセル)のin vivo【動物実験】状態を再現した。図1Aに示すように、シアリダーゼで処理したA549細胞の表面のシアル酸のレベルは、シアリダーゼで処理した細胞は、未処理の細胞よりも低かった(図1A)。
COVID-19スパイクタンパク質に特異的な7つのヒトモノクローナル抗体(表1)を用いて、A549細胞との結合性を調べた。図1Cに示すように、7つのうち2つ(28.6%)の、REGN1098717およびB3815が、シアル酸が欠損したダメージを受けたA549細胞に強く結合した。
シアル酸が欠損した損傷を受けたA549細胞に強く結合した。REGN10987は健常なA549細胞には弱く結合したが、38は健康なA549細胞には結合しなかった(図1B)。
コントロール抗体であるCR3022-b620は、健常なA549細胞にもダメージを受けた細胞にも結合しなかった。(図1Bおよび1C)。
他の4つのヒトモノクローナル抗体は健全なA549細胞にもダメージを受けた細胞にも有意に結合しなかった。
さらに、SARS-CoVウイルスのスパイク糖タンパク質に特異的な抗体は(抗SARS S)が強く結合した。
シアル酸を欠損したダメージを受けたA549細胞には強く結合したが、シアル酸を有する健康なA549細胞には結合しなかった。
シアル酸を持つ健常者のA549細胞には結合しなかった(図1E)。
さらに、ヌクレオキャプシド(N)タンパク質に特異的なポリクローナル抗体であるCOVID-19ウイルス(抗COVID-19 N)と、SARSのヌクレオカプシドタンパク質に特異的な抗体であるSARS-CoVウイルスのヌクレオカプシドタンパク質に特異的な抗体(抗SARS N)健康なA549細胞にも、ダメージを受けた細胞にも有意に結合しなかった。
損傷した細胞にも有意に結合しなかった(図1Dおよび1E)。同様の結果は、腎臓の胚細胞であるHEK-293でも観察された。
HEK-293でも同様の結果が得られた(データは示していない)。以上のことから、in vitro【試験管内】試験の結果は
COVID-19およびSARS-CoVウイルスのスパイクタンパク質に特異的な抗体は、免疫系を惑わせて宿主を攻撃する可能性があることを示している。
ヒトの肺上皮細胞などの病気の細胞に結合することで肺上皮細胞などの病気の細胞に結合することで、免疫系を誤認させて宿主を攻撃する可能性がある。私たちは、この抗体の作用メカニズムを私たちは「抗体依存型自己攻撃[Antibody Dependent Auto-Attack](ADAA)」と名付けた。
REGN10987の抗体は、病気の細胞だけでなく、健康な細胞にも低い割合で結合するため、生体内の免疫反応を活性化することで、より高いADAA能力を発揮すると考えられる。
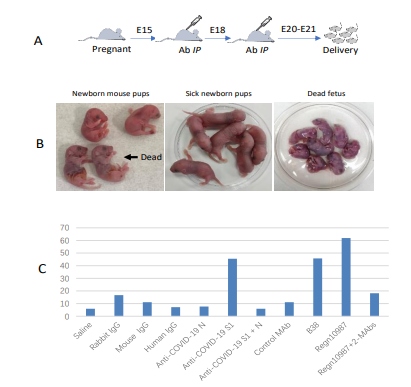
図2. 時限的に妊娠したマウスモデルで
A:妊娠マウスに抗コロナウイルス抗体を注入する手順。
B:抗体を注入した雌マウスから生まれた仔マウスの代表的な画像。
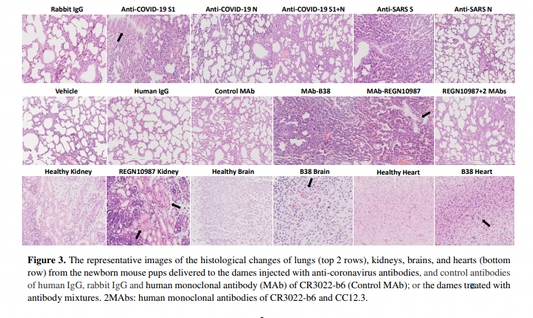
C:抗コロナウイルス抗体による仔マウスの病死率と、抗体の治療効果 抗S1抗体と抗N抗体の混合物、または REGN10987にCR3022-b6を加えたものと CC12.3(2-MAbs)を使用した。動物実験により、抗COVID-19スパイク抗体を単独で投与すると全身の炎症や損傷を引き起こすことがわかった。さらなる確認のため、ウイルス感染のない時限妊娠マウスモデルを使用した。
胎児の臓器の表面糖タンパク質は完全に発達していないか、未成熟であるため、ウイルス感染のない時限妊娠マウスモデルを使用した。マウスモデルには、REGN10987とB38の抗COVID-19 S1、抗COVID-19 N、抗SARS、抗SARS N、ヒトモノクローナル抗体の精製されたエンドトキシンフリーのIgG(表1)を使用した。ウサギ、マウス、ヒトの健常者血清の精製されたエンドトキシンフリーのIgG、およびモノクローナル抗体CR3022-b6をコントロールとして使用した。各抗体IgGの2つの投与量を、妊娠中のマウスに3日おきに2回、腹腔内(IP)に注射した。
エンブリオニック)日 E15およびE18において、それぞれ方法に記載されているように (とした(図2A)。)
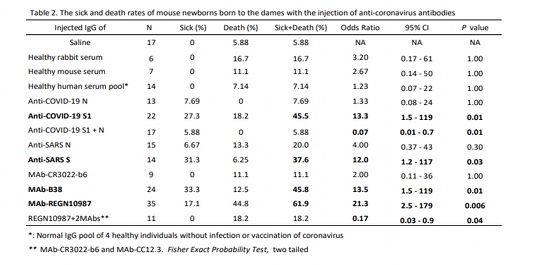
胎児の病気や死亡の頻度と 胎児と新生児の病気と死亡の頻度を表2と図2Cにまとめた。図2C 妊娠中のマウスにREGN10987を注射すると 妊娠中のマウスにREGN10987を注射すると、出産したマウスの子犬が有意に胎児死亡および新生児死亡した。胎児および新生児の死亡が認められた(表2)。この 胎児の死亡は剖検により確認された(図2B)。これらの結果から この動物モデルの結果から、REGN10987は REGN10987が最も高い確率で病死を誘発することがわかった。次いでB38(45.8%)、ポリクローナル抗COVID-19 S1(45.8%)であった。およびポリクローナル抗COVID-19 S1(45.5%)であった。また また、ポリクローナル抗SARS Sは、新生児のマウスに重大な病気 新生児マウスの仔では37.6%が死亡した。また さらに、左上下肢末端の充血 1匹の仔の左目の横に小さな血管腫が観察されました。観察された。この子は、ポリクローナル抗COV抗体を注射された雌犬から生まれました。ポリクローナル抗COVID-19 S1抗体を注射した女性から生まれた子犬であった。健常対照抗体、抗COVID-19 N抗体、抗COVID-19 S1抗体のいずれも使用しなかった。抗COVID-19 Nおよび抗SARS Nのいずれもが仔マウスに重大な病気や死をもたらすことはなかった(表2)。
驚くべきことに、病原性ポリクローナル抗COVID-19 S1抗体と非病原性抗COVID-19 Nを同量(50g + 50 g)、抗体混合物によって誘発される病気と死亡率は に比べて有意に低かった。抗COVID-19 S1の単独投与に比べて有意に低かった(表2)。
さらに、高病原性のREGN10987によって誘発される病死率は 病原性の高いREGN10987抗体による病死率も また、病原性の高いREGN10987抗体による病死率は、同抗体と他の 非病原性の2つの抗体、CR3022-b6および CC12.3、を注入した(表2)。混合物の構成はREGN10987が40g、CR3022-b6が20g、CC12.3が20gであった。
このデータは、非病原性の抗体を共存させることで非病原性抗体の共存は、病原性抗体の病原性を低下させることが示唆された。組織学的変化
仔マウスの肺、脳、心臓、腎臓、腸、肝臓の組織切片を、組織切片をヘマトキシリン・エオジン(HE)で染色し,組織学的評価を行った。生体内で組織に結合したヒトIgGまたはウサギIgGは、蛍光標識した抗ヒトIgG、または抗ウサギIgGを二次抗体として免疫蛍光染色により検出した。
肺の炎症と傷害 急性肺炎
抗COVID-19 S1, 抗SARS S, REGN10987, とB38を注射した雌マウスから生まれた仔マウスの組織をHE染色したところ、肺炎が観察された(図3)。肺病変は、肺の 肺うっ血、肺胞上皮の過形成と肥厚 肥厚、出血、肺胞閉鎖、肺胞拡張、肺胞病変などが見られた。肺胞融合が見られた(図3および図S1)。局所病変部での炎症細胞の浸潤も観察された。
炎症細胞の浸潤も観察された。肺の組織学的変化は軽微なものであった。肺の組織学的変化は軽微であった。の抗体を注射した雌犬から生まれた仔犬の肺には、軽微な組織学的変化が見られた。抗COVID-19 N、抗SARS N、CR3022-b6、および対照のヒト、ウサギのIgGを注射した雌犬の肺には、軽微な組織変化が見られた。コントロールのヒト、ウサギ、マウスのIgGを注射した子犬の肺に変化が見られた(図3)。その他の臓器の炎症と傷害
前述のように、マウスの仔の腎臓、脳、心臓の組織でも炎症反応や出血が見られた。抗COVID-19 S1、抗SARS S、B38、REGN10987を投与したマウスの仔の腎臓の組織は、急性の尿細管損傷を示した。腎尿細管上皮細胞は、顆粒状または空胞状の変性、管腔の拡張または閉塞、少量の炎症細胞の浸潤を伴う腎間質の浮腫を示し、上皮細胞の一部は脱落した(図3およびS2)。REGN10987による腎障害は最も顕著であった(図3)。さらに、抗COVID-19 S1、抗SARS S、B38、およびREGN10987の抗体を注射した飼い主に引き渡されたマウスの仔の脳には、少量の脳出血や炎症細胞の浸潤が観察された(図3およびS2)。さらに、抗COVID-19 S1、抗SARS S、およびB38を注射したデイムに引き渡されたマウス仔の耳には、心筋の出血が見られた(図3およびS2)。最後に、B38の抗体を注射した飼い主に引き渡されたマウスの子犬では、心筋の腫れと炎症細胞の浸潤が観察された(図3)。また,抗COVID-19 N,抗SARS N,CR3022-b6,コントロールIgG(ヒト,ウサギ,マウス)の抗体を注射したマウスの仔の組織では,組織学的変化はほとんど見られなかった。これらの結果から、COVID-19やSARS-CoVなどのコロナウイルスのスパイクタンパク質に特異的な抗体は、抗体依存性自己攻撃(ADAA)のメカニズムにより、胎児や新生児の死亡、肺などの全身の炎症や損傷を引き起こすことが証明された。
胎児や新生児の死亡、肺やその他の臓器の全身的な炎症や損傷を引き起こす。この結果は、COVID-19患者の臨床観察結果と一致している
重症化にしたがって、抗COVID-19 S1、抗SARS-CoV S、B38、およびREGN10987の特定の抗体は病原性を持ち、ADAAを誘発する。これらの重篤なCOVID-19感染症の重篤な状態は、この病原性抗体とADAAが原因であると考えられる
COVID-19感染症の一方で、このようなティボディ 抗COVID-19 N、抗SARS-CoV N、およびCR3022-b6の抗体は CR3022-b6は、生体内で有意な副作用を誘発しなかったことから、非病原性であると考えられる。炎症性サイトカイン
抗スパイク抗体の病原性のさらなる証拠として、マウス仔の血清中のオノサイトケモタクティックプロテイン1(MCP-1)、腫瘍壊死因子-(TNF-)、インターロイキン-4(IL-4)、IL-6、およびIL-10のサイトカインレベルを、マルチフレックス Luminex アッセイキット(Millipore社製)を使用した。
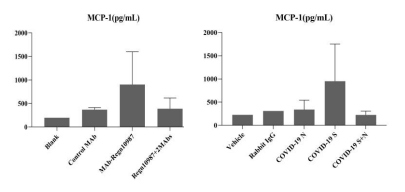
メーカーの指示に従った。MCP-1の結果を図4にまとめた。
病原性の抗COVID-19 S1とREGN10987の両方が、有意に高いレベルのMCP-1を誘導した(図4)ところ、驚くべき結果と一致した。
病原性抗COVID-19 S1と非病原性抗COVID-19 Nからなる混合抗体を用いた治療は、抗COVID-19 S1単独で誘導されたものと比較して、MCP-1のサイトカインレベルを有意に減少させた(P < 0.001)(図4)。さらに、病原体であるREGN10987と非病原体であるCR3022-bの2つの抗体からなる混合抗体を投与したところ、MCP-1が有意に減少した。
また、病原体であるREGN10987と、非病原体であるCR3022-b6およびCC12.3の2つの抗体からなる混合抗体を投与すると 顕著な MCP-1のレベルを有意に低下させた(P < 0.001)。REGN10987の単独投与に比べて有意に減少した(図4)。他のサイトカインの 他のサイトカインのレベルは有意に上昇しなかったが、これはおそらく仔マウスの免疫力が未発達であったためと思われる。
この結果は 疾病率、死亡率(表2)および組織学的変化(図3)の結果と一致した。および組織学的変化(図3)と一致した。これらのデータ 1) 病原性抗体のみでも 高濃度の炎症性サイトカインを誘導し、サイトカインストームやサイトカイン放出症候群(CRS)を引き起こす可能性があること、放出症候群(CRS)を引き起こす可能性があること、非病原性抗体が共存することで、病原性抗体によって誘発される炎症性サイトカインの放出を抑えて 病原性抗体によって引き起こされるサイトカインストームやCRSを防ぐことができる。仔マウスの複数の臓器に対する動物実験での抗体結合
抗COVID-19スパイク抗体の病原性ADAAを示す証拠として、仔マウスの組織への動物実験での抗体結合を記載したように免疫蛍光染色で検出した。
図4. 新生児マウス血清中のMCP-1のサイトカインレベル
マウス血清中のサイトカイン濃度
仔マウスの血清中のMCP-1濃度
抗体を単独で注射した雌犬と
抗体を単独で注入した場合と
抗体混合物ヒトとウサギの抗COVID-19スパイク抗体は、肺、腎臓、脳の炎症部位や病変部位で有意に検出された。(図5)
これらの仔マウスは病原体である抗COVID抗体を注射した雌マウスに引き渡した。
抗COVID-19 S1抗体、抗SARS-CoV S, REGN10987、B38を注射した(図5)。ヒトIgGもウサギIgGも検出されなかった。
非病原性抗体である抗COVID-19 N, 抗SARS N, CR3022-b6(が検出された(図5)。) この結果から、特定の抗COVID-19スパイク抗体は、胎盤を通過して胎盤を通過し、胎児の組織に結合し、自己攻撃免疫反応を活性化して自己攻撃型の免疫反応を活性化し、全身の肺、腎臓、心臓などの多臓器に組織的な炎症や損傷を引き起こすことがわかった。この結果は
組織学的変化と一致し(図3) 動物実験で病原性を示す証拠となりました。
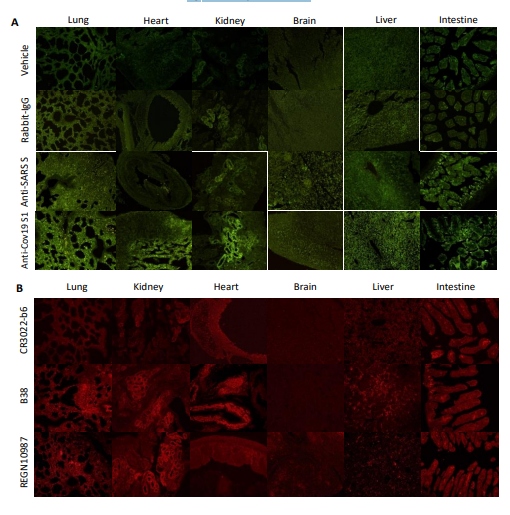
COVID-19ウイルスおよびSARS-CoVウイルスの一部の抗スパイク抗体のADAAの病原性を示す生体内の証拠となった。ヒトおよびウサギの抗COVID-19スパイク抗体は、重症化した仔マウスの肺、腎臓、脳、心臓、肝臓、腸の組織の炎症部および病変部で有意に検出された(図5)。
これらのマウスの仔は、抗COVID-19 S1、抗SARS-CoV S、REGN10987、B38の病原性抗体を注射したデイムに引き渡された(図5)。
非病原性抗体である抗COVID-19 N、抗SARS N、CR3022-b6を投与した仔マウスの組織では、ヒトIgGもウサギIgGも有意に検出されなかった(図5)。
この結果は、特定の抗COVID-19スパイク抗体が胎盤を通過して胎児の組織に結合し、自己攻撃型の免疫反応を活性化し、肺、腎臓、心臓、脳などの複数の臓器に組織的な炎症と傷害をもたらしたことを示している。この結果は、組織学的変化(図3)の結果と一致しており、COVID-19ウイルスおよびSARS-CoVウイルスの一部の抗スパイク抗体の病原性ADAを動物実験で証明することができた。
図5. E15およびE18に抗体を注入したデイムから生まれた仔マウスの多臓器の病変部に生体内で結合した抗コロナウイルス抗体の検出。重症化したマウスの仔の心臓、肝臓、腸を採取した(図5)。
これらのマウスの仔は、抗COVID-19 S1、抗SARS-CoV S、REGN10987、B38の病原性抗体を注射したデイムに引き渡された(図5)。非病原性抗体である抗COVID-19 N、抗SARS N、CR3022-b6を投与した子犬の組織では、ヒトIgGもウサギIgGも有意に検出されなかった(図5)。この結果は、特定の抗COVID-19スパイク抗体が胎盤を通過して胎児の組織に結合し、自己攻撃型の免疫反応を活性化し、肺、腎臓、心臓、脳などの複数の臓器に組織的な炎症や傷害をもたらしたことを示している。この結果は、組織学的変化の結果と一致しており(図3)、COVID-19ウイルスやSARS-CoVウイルスの一部の抗スパイク抗体の病原性ADAを動物実験で証明した。病原性抗体の胎児組織および疾患組織への結合 病原性抗COVID-19スパイク抗体のヒトにおける病原性をさらに評価するために、最も高い病原性を持つREGN10987を用いて、様々なヒト胎児組織、または組織アレイスライド(US Biomax)から得た複数のヒト疾患組織への抗体結合を試験した。その結果を図6に示す。
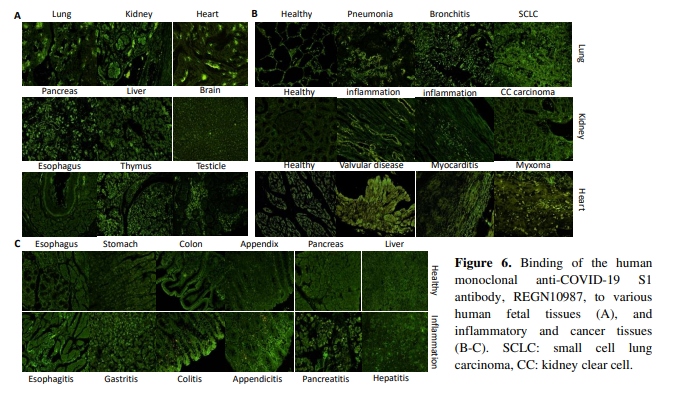
抗体REGN10987は、肺、心臓、腎臓、脳、膵臓、肝臓、胸腺、精巣などの複数のヒト胎児組織に結合したが、食道には結合しなかった(図6A)。さらに、REGN10987は、網膜とコロイド、強膜、眼球の胎児組織にも結合した(データは示していない)。このデータは、未成熟な胎児組織が、腎臓 車 肺 心臓 脳 肝臓 腸 抗SARS S 抗Cov19 S1 Rabbit-IgG A B38 REGN10987 肺 腎臓 心臓 脳 肝臓 腸 CR3022-b6 B 図5.
REGN10987などの病原性抗体をE15およびE18に抗体注射して生まれたダミーの仔マウスの多臓器の病変部にin vivoで結合した抗コロナウイルス抗体の検出。さらに、REGN10987は、ヒトの呼吸器系、循環器系、泌尿器系、消化器系の炎症組織やがん組織にも広く結合した(図6B-6C)。
炎症組織は、肺炎、気管支炎、気管支拡張症、弁膜症、リウマチ性弁膜症、心筋炎、食道炎、胃炎、胆嚢炎、虫垂炎、膵臓炎、肝炎などの患者のものであった。癌組織は、小細胞肺癌、腎明細胞癌、粘液腫の患者のものだった。この結果から、炎症組織や癌組織など、活発に増殖している細胞や組織の多くは、REGN10987のような病原性のある抗COVID-19 S1抗体に対して脆弱であることが判明した。
図6. ヒトモノクローナル抗COVID-19 S1抗体であるREGN10987の様々なヒト胎児組織(A)、炎症組織や癌組織(B-C)への結合性。SCLC:小細胞肺がん、CC:腎明細胞。
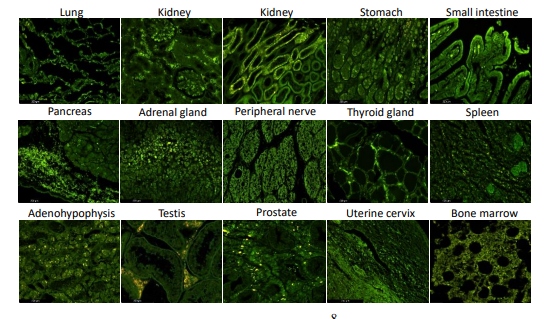
図7. REGN10987の様々なヒト正常組織への結合病原性抗体のヒト健常組織への結合 病原性抗COVID-19 S1抗体の病原性をさらに評価するために、REGN10987と組織アレイスライド(US Biomax, FDA999w)からの複数の健常ヒト組織を用いた。この組織アレイスライドは、FDAの抗体交差反応性試験のガイドラインに沿って、ヒトのほとんどの組織を網羅する32種類の正常なヒトの臓器から構成されている。その結果、REGN10987は、ヒトの健常組織である肺、腎臓、膵臓、胃、腸、副腎、末梢神経、甲状腺、脾臓、下垂体、精巣、前立腺、骨髄、がんの隣接する正常組織である子宮頸部に有意に結合した(図7)。さらに、REGN10987は、副甲状腺、心膜中皮、眼の隣接する正常な強膜の組織にも結合した(データは示されていない)。これらのデータは、REGN10987のようなある種の抗COVID-19 S1抗体は、健康なヒトの組織に結合し、自己攻撃型免疫反応(ADAA)を活性化し、生体内で重篤な有害反応を引き起こす可能性が高く、高い病原性を有することを示している。今回の結果から、COVID-19感染時に病原性抗体を臨床的に検出することは、重篤な感染症を発症した患者の結末を予測するのに役立つと考えられる。
今回の研究の試験管および動物実験のデータを総合すると、COVID-19スパイク・タンパク質に特異的な特定の病原性抗体が重篤なCOVID-19感染症の原因となり、ADAAを介してCOVID-19感染症の際に重篤な合併症を引き起こす可能性があることが明らかになりました。さらに、病原性抗体は、成熟していない胎児の細胞または組織に結合し、妊娠中の女性の流産、産後の陣痛、死産、および新生児の死亡を引き起こす可能性がある。
なお、本研究のモノクローナル抗体のデータによると、病原性抗体は全体の30%以下であるため、COVID-19ウイルスによって誘導される抗COVID-19スパイク抗体の大部分(70%以上)は非病原性であることがわかっている。
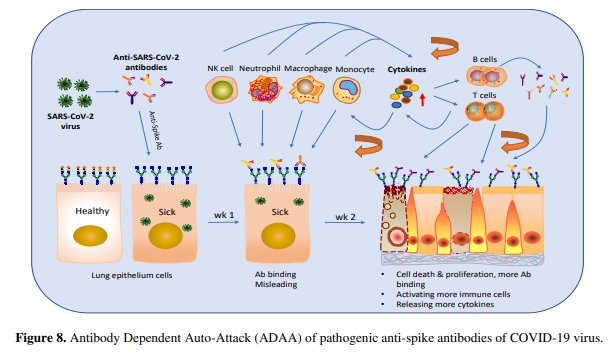
図8. COVID-19ウイルスの病原性抗スパイク抗体のADAA(Antibody Dependent Auto-Attack)。考察
今回の研究では,COVID-19ウイルスやSARS-CoVウイルスなどのコロナウイルスのスパイクタンパク質に特異的なある種の抗体の病原体としての役割と新しい作用機序(ADAA)を明らかにした(図8)。私たちは、マウスモデルにおいて、抗インフルエンザ免疫血清を事前に投与すると、インフルエンザウイルスのみを感染させたマウスよりも重篤な感染症を引き起こすことを発見していた14。Wangらは,抗SARS-CoVスパイク抗血清が,in vitro【試験管内】で抗体依存性増強(ADE)によりSARS感染を促進することを報告した22.Liuらは、SARS-CoVワクチンによって誘導された抗SARS-CoVスパイク免疫血清が、SARS-CoV感染マカクモデルにおいて、MCP1およびIL-8の産生、単球またはマクロファージの動員および集積を促進することで、急性肺傷害を引き起こすことを報告した。
これまでに報告されているこれらの抗スパイク抗体の作用機序(MOA)は、抗体がウイルスの感染力を増強するというADEベースのものである24。今回の研究では、病原性抗体が宿主の脆弱な細胞や組織に結合し、免疫反応を誤らせて宿主自身を攻撃するという、自己細胞を標的とした作用機序を初めて明らかにした(ADAA)。また、本研究では、高病原性ウイルス感染症の新たな病原性メカニズム(MOP)を解明しました。このMOPは、COVID-19ウイルスやSARS-CoVウイルスなどの高病原性ウイルスが誘導する病原性抗体によって引き起こされる。さらに、この病原性抗体は、ADAAを介して、COVID-19ロングホーラーを含む感染症関連自己免疫疾患の原因に関係している可能性がある。
抗ウイルス抗体の二重の役割 伝統的な概念に基づけば、感染性病原体によって誘導される抗体は、病原体を中和し、感染症を予防または治療することができるため、宿主にとって保護的である。しかし、このような抗体の役割は二面性を持っている。理論に縛られることなく、私たちは、一部の抗体が宿主の細胞や組織と交差反応し、自己細胞や自己組織を攻撃する免疫反応を引き起こす可能性があることに気づいた(ADAA)。
今回のデータでは、COVID-19ウイルスやSARSウイルスの抗スパイク抗体がそのような病原性を持つことが示された。シアル酸は、細胞膜の外側にある粘膜の優勢な構成要素であり、主に生物学的マスクまたは受容体として作用する25。シアル酸を持つ細胞や組織は「自己」として認識される25。シアル酸が失われると、細胞構造は「非自己」25となり、免疫反応を活性化させることができる。また、シアル酸は、コロナウイルスやインフルエンザウイルスなど、いくつかのウイルスの受容体の重要な付着分子でもある25,21。このようなウイルスに感染すると、肺上皮細胞などの感染細胞上のシアル酸は、COVID-19ウイルスなどのコロナウイルスの受容体破壊酵素(RDE)や、インフルエンザウイルスのシアリダーゼによって除去・破壊される可能性がある。細胞表面のシアル酸が欠損したダメージを受けた細胞は、ウイルスが誘導する病原性抗体に対して脆弱になる(図8)。
例えば、今回の研究では、SARS-CoV-2スパイクとSARS-CoVスパイク糖タンパク質に特異的な抗体が、細胞表面のシアル酸が欠損した損傷した肺上皮A549細胞(図1)や腎臓胚HEK-293細胞に有意に結合することが示された。この抗体の結合は、自己を攻撃する免疫反応を活性化させたり、誤解させたりして、生体内の多臓器の傷害を誘発する可能性がある。例えば、COVID-19 S1やSARS-CoV Sタンパク質に特異的な抗体を妊娠中のマウスに注射すると、図1-4や表2に示すように、胎児や新生児の死亡や、ダミーで生まれたマウスの仔の複数の臓器の傷害が誘発された。一方、非病原性の抗体である抗COVID-19 Nおよび抗SARS Nは、生体内で大きな傷害を誘発しなかった。
抗COVID-19 N抗体も抗SARS N抗体も、健康なA549細胞にも損傷を受けたA549細胞にも有意に結合しなかった(図1E)。
胎児モデルを選択したのは、表面の糖タンパク質を含む多くの胎児組織が未成熟であり、病原性抗体に対して脆弱であるためである。
COVID-19のS1(S-RBD)タンパク質に特異的な7つの天然由来のヒトモノクローナル抗体15,16,17,18,19,20について、上述のin vitroアッセイを用いて、その病原性を分析した。その結果、1つ(85.7%)を除くすべての抗体が、健常なA549細胞に結合しなかった。しかし、B38とREGN10987の2つの抗体(28.6%)は、損傷したA549細胞に有意に結合した(図1C)ため、病原性の可能性のある抗体として選択し、in vivoの動物モデルでさらに確認した。ウイルスフリー動物実験の結果、図1〜4および表2に示すように、この2つの抗体だけでも高い病原性を示し、ダミーマウスから生まれた仔マウスの胎児および新生児の著しい死亡や複数の臓器の損傷を誘発した。
一方、7つのモノクローナル抗COVID-19 S1抗体のうち、もう1つの抗体であるCR3022-b6はコントロール抗体として機能し、in vivoで有意な傷害を誘発しなかった(図1-4および表2)。これらのデータから、in vitroアッセイは潜在的な病原性抗体の迅速なスクリーニングに有用であり、ウイルスフリーの動物モデルはこれらの特定の抗体の病原性の確認に有用であることが示された。なお、病原性抗体が母親の組織に結合した場合、マウス胎児への影響が軽減される可能性があることに留意すべきである。
病原性抗体は、COVID-19感染症などの高病原性感染症の際に誘発される可能性がある。病原性抗体とそのADAA機構の発見は、ウイルス感染症、特にCOVID-19感染症のような病原性の高いウイルス感染症の重篤な感染症、重篤な合併症、後遺症が発生する可能性のある病因メカニズム(MOP)の謎を解明する可能性がある。このことは、サイトカインストームやサイトカイン放出症候群(CRS)の原因や、感染症関連の自己免疫疾患(COVID-19ロングホーラー26が患ったものも含む)、感染症関連の癌、その他病原性抗体によって誘発される可能性のある障害についても説明できるかもしれません。病原性抗体によって引き起こされる病気や状態には、さらに、感染症に関連した妊娠中の女性の流産、産後の陣痛、死産、新生児死亡が含まれる。ウイルス感染症の新たな発症メカニズム 今回の研究のin vitroおよびin vivoのデータは、COVID-19ウイルスのような高病原性ウイルスの新たなMOPを支持するものである。このMOPには COVID-19ウイルスのような高病原性呼吸器ウイルスは、標的となる臓器に局所的な炎症やシアル酸が欠損した細胞損傷などの初期の一次傷害を引き起こす。
COVID-19ウイルスなどの高病原性呼吸器ウイルスが、感染後1週間以内に、肺などの標的臓器に局所的な炎症やシアル酸欠損を伴う細胞損傷などの最初の一次傷害を引き起こすこと、2)1週間目から病原性抗体を含む抗ウイルス抗体が上昇すること。病原性抗体は、標的臓器(例えば肺)の損傷した細胞や炎症を起こしている細胞に結合する(図8)。肺など)に結合し(図8)、また同様の損傷を受けた他の臓器(腎臓、脳、心臓など)にも結合する。3) 抗体の結合は、自己の細胞や組織を攻撃するように免疫反応を活性化させ、誤った方向に導き(ADAA)、さらなる損傷(二次的な損傷)を誘発する。4) 二次的な損傷は、一次的な損傷にさらなる損傷を持続的に加え、雪だるま式に増えていき、1週目から2〜3週目にかけて抗体がピークレベルに達すると、ARDS、サイトカインストーム、さらには死などの重篤な状態を引き起こす(図8)。および5)病原性抗体に惑わされた自己攻撃型免疫反応(ADAA)は持続性があり、ウイルスクリアランス後も抗体が存在し続ける限り蓄積し、自己免疫疾患を引き起こす可能性がある。
一次感染は限定的で短く、通常のインフルエンザ感染で見られるように、ウイルスが除去されるにつれて減少する。
つまり、ウイルス自体はARDS、サイトカインストーム、死亡などの重篤な状態を引き起こすのに十分ではないということになる。一方、病原性抗体による二次災害は、ウイルスよりもはるかに長く持続し、肺以外の炎症組織や臓器にも非特異的に結合するため、より長く、より広く、より付加的なものとなる。このように、病原性抗体によるADAA反応が重なり合うと、ARDS、サイトカインストーム、死などの重篤な状態に陥る可能性がある。COVID-19感染症や高病原性インフルエンザ感染症などの重篤な呼吸器系ウイルス感染症の患者の大半が1週目以降、特に感染コースの2〜3週目に死亡した理由3,27は、抗体レベルがピークに達する時期と一致していることから、この新しいMOPで説明できる。また、この新しいMOPは、1918年のインフルエンザパンデミックで重症または致死的な感染の大半が若年層に起こった理由を説明することができる。これは、若年層が病原性抗体を含むより高いレベルの抗ウイルス抗体を誘導することができたからである。
同様に、インフルエンザウイルスなどの他の感染性病原体によって誘導される特定の病原性抗体も、このMOPを介して重篤な副作用や自己免疫疾患を引き起こす可能性がある(研究継続中)。病原性抗体に脆弱な細胞や組織 図6に示すように、高病原性のREGN10987抗体は、大部分のヒト胎児組織や炎症組織、さらに特定の癌組織に結合した。癌組織を含むそれらの組織の共通の特徴は、活発に増殖する細胞で構成されていることである。そのため、それらの細胞や炎症組織は病原性抗体に対して脆弱であり、病原性抗体(ADA)との相互作用は、1)重篤な感染症、特にCOVID-19感染症などの高病原性ウイルス感染症、2)ARDS、サイトカインストーム、サイトカイン放出症候群(CRS)などの感染症の重篤な合併症、3)肺炎や腎不全などの感染症関連の炎症などの原因となる(図1-4)。さらに、成熟していない胎児の細胞や組織は、病原性抗体に対して脆弱である(図6A)。このように、ADAAを介した病原性抗体は、妊娠中の女性の流産、産後の陣痛、死産、新生児死亡の原因となっている可能性がある(図1B、1C)。
病原性抗体と自己免疫疾患 自己免疫疾患の多くはウイルス感染と関係している28が、その発症メカニズムはこれまで不明であった。今回の研究で、ほとんどの炎症組織が病原性抗体やADAAに対して脆弱であることが初めて明らかになった(図6B)。ほとんどの自己免疫疾患では、慢性的な炎症が見られる。感染症が発生すると、病原性抗体を含む抗体が誘導され、数ヶ月から半年程度持続する。
病原性抗体は、自己免疫疾患の既存の脆弱な炎症組織に容易に結合し、免疫反応を誤らせて自分の組織を攻撃してしまう。このADAAのプロセスは、抗体が上昇して重大な反応を誘発するため、反復的かつ加算的になる。病原抗体とADAAによって引き起こされる自己免疫疾患の発生時間と発症経過は、脆弱な細胞や組織の量と病原抗体の量に応じて、短くも長くもなる。病原抗体は一般的に数ヶ月から半年程度持続するため、その間、特に抗体量がピークに達する時期に自己免疫疾患が発症することがある。
COVID-19のロングホーラーが報告されているが、その原因は謎のままである。今回の研究では、COVID-19 long haulersの発症メカニズムの可能性が示されました。回復したCOVID-19患者ではウイルスが除去されたにもかかわらず、抗ウイルス抗体が残り、数か月から半年以上も存在する可能性がある。
ある種の病原性抗体は、COVID-19感染時に誘発された炎症細胞などの脆弱な細胞や組織に結合し、持続的な多臓器の慢性炎症などの持続的な有害反応を引き起こす可能性がある。このように、ADAAのメカニズムでは、病原性抗体もCOVID-19の感染による長期的な影響の原因となり得る。
例えば、REGN10987のような病原性の高い抗スパイク抗体は、末梢神経に結合し、筋肉や視覚、味覚などの異常を引き起こす可能性がある。
同様に、鳥インフルエンザウイルスなどの他の感染性病原体によって誘導される病原性抗体は、ギラン・バレー症候群(GBS)などの感染症による副作用や自己免疫疾患の原因となる。また、HIVなどの慢性ウイルス感染症では、病原性抗体が長期間にわたって細胞増殖を繰り返し促し、細胞増殖がコントロールできなくなると、感染症に起因するがんが発生することがある。
より優れたワクチン
病原性のある抗COVID-19 S1抗体に、同量の非病原性の抗COVID-19 N抗体を混合したところ、抗COVID-19 S1抗体を単独で注射した場合に比べて、混合抗体による病気や死亡率が大幅に減少したことは驚異的だった(表2、図1C)。同様の結果は、高病原性のREGN10987でも、REGN10987とCR3022-b6およびCC12.3の2つの非病原性モノクローナル抗体を混合した抗体でも観察された(表2および図1C)。このデータから、非病原性の抗体を共存させることで、病原性の抗体のADAAを低減できることが示唆された。このように、多価の抗体を誘導できるワクチンは、少なくとも1種類の抗体が、より少ない副反応を誘導する非病原性の種類である方が安全であると考えられる。このようなワクチンの一例として、ウイルスの複数の抗原に特異的な多価抗体を誘導する従来の不活化ウイルスワクチン(例えば、不活化COVID-19ワクチン)が挙げられる。別の例として、SARS-CoV-2ウイルスのスパイクタンパクだけでなく、ヌクレオカプシドタンパク、または非スパイクタンパクに特異的な抗体を誘導することができる組換えまたはmRNAのCOVID-19ワクチンは、より安全性が高いと考えられる(特許出願中)。作用機序は不明であるが、抗COVID-19 S1も抗COVID-19 Nも同じ抗原に結合しないことから、非病原性抗体が競合結合によって病原性抗体のADA作用に影響を与えたとは考えられない。
REGN10987も他の2つの非病原性抗体も、COVID-19ウイルスのS1タンパク質の同じエピトープに結合しない。非病原性抗体は、病原性抗体が脆弱な細胞や組織に付着するのを希釈したり、空間的に妨害したりすることで、病原性抗体のADAに影響を与えているのではないかと考えられる。
新たな発症メカニズムに基づく新規臨床介入 病原性抗体によって誘導される高病原性ウイルス感染症の新たなMOPに基づき、病原性抗体の宿主の脆弱な細胞・組織・臓器への結合を阻害することで、COVID-19感染症の重篤な病態を治療・予防するための新規臨床介入薬が開発される可能性がある。
例えば、重篤なCOVID-19感染症の治療には、以下のような製品やアプローチが有効であると考えられる。
1) 重篤な状態にある患者に対しては、患者の血漿を感染していない健康なヒトの血漿と交換するなど、病原性抗体を除去することができる治療法が有効な場合があり、可能な限り早急に実施されるべきである。
2)回復した患者だけでなく、健康な人から採取した免疫グロブリン製剤、血清、血漿は、病原性抗体の結合を希釈・遮断することで症状の緩和に役立つ可能性があること。
3)ウイルス抗原や抗原断片、合成ペプチドなどの病原体由来の製品が有効である可能性があること(病原性抗体の中和)(特許出願中)などが挙げられる。重篤なCOVID-19感染症の診断には、抗COVID-19スパイク抗体のレベルを決定することが重要であり、重篤な感染症患者の状態を予測するのに役立つ。なぜなら、ウイルスは1週間後には検出されなくなるが、ウイルスによって誘導される抗体は1週間目から上昇し、2〜3週間目にはピークレベルに達し、ARDS、サイトカインストーム、死亡などの重篤な症状の発症を伴う。
抗COVID-19スパイク抗体の高値は、感染症の悪化を示していると考えられる。
以上のように、今回の研究では、ウイルス感染症における「病原性抗体」の役割が明らかになりました。これらの病原性抗体は、私たちが「抗体依存性自己攻撃」(ADAA)と呼んでいる新しい作用機序で働く。特に、COVID-19などの高病原性呼吸器ウイルス感染症のADAAを調べました。病原性抗体は、感染時に誘導され、活発に増殖している細胞などの脆弱な細胞や組織に結合し、持続的な自己攻撃免疫反応を開始し、ARDS、サイトカインストーム、死などの重篤な症状を引き起こす。さらに、ADAAを介した病原性抗体は、COVID-19ロングホーラーが経験するような感染症関連の自己免疫疾患にも関与している可能性がある。病原性抗体のADAAに基づく改良型ワクチンを含む、診断と治療のための新しい臨床介入が開発される可能性がある。また、本研究で検討された新しい概念とADAAのメカニズムは、高病原性インフルエンザ感染症などの他の感染症にも適用できる可能性がる(研究継続中)。
手法
ヒト抗SARC-CoV-2スパイクモノクローナル抗体の作製 SARS-CoV-2ウイルスのスパイクタンパク1(S1)の受容体結合ドメイン(RBD)に特異的な7つの天然由来のヒトモノクローナル抗体が他の研究者によって報告されている15,16,17,18,19,20。
7つのモノクローナル抗体は、NCBIの結晶構造サイトの遺伝子配列に従って、研究用にのみ複製されたものである(HuaAn McAb Biotechnology)(表1)。抗体の特徴と情報を表1に示す。抗Spikeヒト抗体の重鎖と軽鎖のペアのプラスミドを、ポリエーテルイミド(Polysciences社)を用いて1:2の質量比でHEK-293FE細胞に一過性にトランスフェクトした。トランスフェクションされた細胞は、5%CO2含有雰囲気下、37℃で懸濁培養し、トランスフェクションから8時間後に条件培地(Gibco社)をリフレッシュした。7日後、上清を10000r/min(rpm)で遠心分離し、Protein A prepacked column(Senhui Microsphere Technology)で精製した。精製された抗体は、NanodropまたはBCA Quantification Kit(Beyotime社)により定量した。抗体の品質管理は、抗原ダウンELISAを用いて行った。COVID-19 Spike-RBD-mFc(HuaAn McAb Biotechnology社)の1g/mlの抗原をELISAプレートに4℃で一晩コーティングした。プレートを1%BSAでブロッキングし、第一抗体として抗スパイクヒト抗体を37℃で1時間ずつ連続してコーティングした。結合していないフリーの抗体をTBSTで洗浄した後、二次抗体であるヒトIgG-HRP(Abcam)をプレートに加え、37℃で30分間インキュベートした。抗スパイクヒト抗体の結合親和性をOD450nmの吸収のサインで分析した。
抗COVID19 Nタンパク質抗体作製 2ヶ月齢のニュージーランド白ウサギに精製COVID19-Nタンパク質250μg((HuaAn McAb Biotechnology))を皮下免疫した。
このウサギには、500gの精製COVID19-Nタンパク質を2週間の間隔で3回ブースター注射した。
抗COVID19-N抗体の血清の力価は、各免疫後に抗原ダウンELISAによって検証された。その後、ウサギの血清を採取し、10,000rpmで10分間遠心分離し、Protein A prepacked column(Senhui Microsphere Technology社)で精製した。精製された抗体は、NanodropまたはBCA Quantification Kit(Beyotime社)により定量した。
抗体溶液からのエンドトキシンの除去 抗体溶液を氷中で1% v/v Triton X-114で10分間処理した。その後、37℃で5分間インキュベートすると、二相が形成された。この抗体溶液を12,000rpmで5分間、室温で遠心分離し、上層の水相を注意深く吸引した。
エンドトキシンフリーの抗体をBCA Quantification Kit(Beyotime社)で定量した。
その他の抗体 SARS-CoV-2ウイルスの組換えスパイク1(S1)タンパク質に特異的なウサギのポリクローナル抗体、SARS-CoVウイルスの組換えスパイクタンパク質に特異的なウサギのポリクローナル抗体、SARS-CoV-2ウイルスの組換えスパイクタンパク質に特異的なウサギのポリクローナル抗体を用いた。
SARS-CoVウイルスの組換えスパイク1(S1)タンパク質に特異的なウサギポリクローナル抗体、およびSARS-CoVウイルスの組換えヌクレオカプシド(N)タンパク質に特異的なマウスモノクローナル抗体は、Bioss
Antibodies社(北京)から購入した。A549細胞のノイラミニダーゼによる消化 ヒト肺上皮細胞株A549の細胞をノイラミニダーゼ用消化バッファー(Roche社)で1回洗浄した後、2000rpmで5分間遠心分離し、上澄みを捨てた。消化バッファーはPBS(pH5.5-6.0)に50mMの酢酸ナトリウム、3%BSA、2mMのCaCl2を加えたものを使用した。各チューブには、50 Uのノイラミニダーゼ(Roche社)を含む200 lの消化バッファーに約106個の細胞が入っていた。このチューブを37℃で1時間インキュベートした。その後、細胞をPBSで1回洗浄し、フローサイトメトリーアッセイに進みました。コントロールとして、ノイラミニダーゼを処理していないA549細胞を用いた。
フローサイトメトリー ノイラミニダーゼを処理したA549細胞または処理していないA549細胞を、上述のように抗コロナウイルス抗体の結合について試験した。200 lの1%BSA-PBS中の各2x105個の細胞を、0.5 mg/mlの濃度の各抗体と氷中で1時間インキュベートし、PBSで1回洗浄した。この細胞を200 lの1%BSA-PBSと0.25 mg/mlのPE標識ヤギ抗ヒトIgG(Abcam)またはFITC標識ヤギ抗ウサギIgG(SouthernBiotech)で再懸濁し、氷中で30分間インキュベートした後、PBSで1回洗浄した。200 lのPBSで再懸濁し、Accuri 6 (BD Biosciences)のフローサイトメーターで検出した。コントロールとして、シアル酸に特異的に結合する蛍光標識小麦胚芽アグルチニン(WGA)(Vector社)を用いた(図1A)。
時限妊娠マウスモデル
抗コロナウイルス抗体の病原作用を評価するために,上記の抗コロナウイルス抗体を用いて,ウイルス感染を伴わない時限妊娠マウスモデルを作成した。動物実験は,杭州師範大学実験動物センターで行った。動物実験のプロトコルは,杭州師範大学の実験動物福祉倫理委員会の承認を得た。CALAS No.は2020244である。動物実験は3回行われた。妊娠(胚)日E13-E14の動物SPFグレードのC57BL/6J妊娠マウスを、上海SLAC実験動物有限公司から購入した。動物は必要に応じてランダムにグループ分けし、実験ごとに各グループ2匹の妊娠マウスを用いた。
抗体注入 動物モデルに使用した抗コロナウイルス抗体の精製されたエンドトキシンフリーのIgGは、ウサギポリクローナル抗COVID-19 S1、抗COVID-19 N、抗SARS-CoV S、マウスモノクローナル抗SARS-CoV N、およびB3815、REGN1098717、CC12.318、CR3022-B620のヒトモノクローナル抗COVID-19 S1またはS-RBD抗体を含む。
各抗体IgGの2つの投与量を、それぞれ妊娠(胚)日であるE15(約26〜28g)およびE18(約30〜32g)の時点で、3日に2回、時限妊娠マウスに腹腔内(IP)注射した(図2A)。各ポリクローナル抗体について、1回目の投与量(約2.0mg/kg)は50μg(マイクログラム)、2回目の投与量(約2.0mg/kg)は60μgを投与した。また、各モノクローナル抗体については、1回目の投与量が40μg(約1.5mg/kg)、2回目の投与量が50μg(約1.5mg/kg)とした。さらに、ウサギポリクローナル抗体混合物として、抗COVID-19 S1を50μg、抗COVID-19 Nを50μg、ヒトモノクローナル抗体混合物として、REGN10987を40μg、CC12.3を20μg、CR3022-B6を20μg、それぞれ投与した。妊娠マウスの体重は、抗体注射の前後に毎日測定した。マウスの仔はE20-E21頃に生まれ、生まれたばかりのマウスの仔の臨床症状を含む健康状態を観察し、記録した(図2B)。生後1-2日目に実験を終了した。サンプル採取 生後1-2日目に新生仔マウスから血液サンプルを採取し,4℃で一晩インキュベートした後,3000rpmで5分間遠心分離し,上清を新しいチューブに移した。分離した血清は、サイトカインの検出のために-80℃で保存した。肺、心臓、脳、腎臓、肝臓、腸を3匹以上のマウスから採取し、ホルマリンで48〜72時間固定した後、アルコール脱水を行い、パラフィンに包埋し、組織切片を作成した。
HEおよび免疫蛍光染色 マウスの肺、心臓、脳、腎臓、肝臓、腸の組織切片を脱脂し、ヘマトキシリン・エオジン(HE)で染色し、組織学的評価を行った。免疫蛍光染色には,脱脂した切片をPE標識ヤギ抗ヒトIgG(Abcam)またはFITC標識ヤギ抗ウサギIgG(SouthernBiotech)の二次抗体と室温で1時間インキュベートし,PBSで3回洗浄した後,免疫蛍光顕微鏡(Leica)で観察した。
組織アレイ 様々なヒト胎児組織(BE01015)、または呼吸器系(LUD151)、心肺系(HE1001)、泌尿器系(BC07014)、消化器系(BCC000128)の複数のヒト疾患組織からなるヒト組織アレイのスライドは、US Biomax(Rockville, MD)から購入した。4-8gのビオチン標識REGN10987抗体を各組織アレイスライドと室温で1時間インキュベートし、遊離抗体を洗い流し、FITC標識ストレパビジンで室温で30分染色し、3回洗浄した後、免疫蛍光顕微鏡(Leica)で観察した。
謝辞
in vitro セルラーアッセイの開発に貴重なアドバイスをいただいた Haifeng Bao 博士、原稿をレビューしていただいた復旦大学の Xiaohui Zhou 博士に感謝します。
に感謝いたします。本研究はHangzhou HuaAn PuChu Investment Limited Partnershipの資金援助を受けています。競業利益
H.W.はHuirui Biopharma社の株主、X.L.およびY.C.はHuaAn PuChu社の株主です。
Y.C.はHuaAn McAb Biotechnologyの株主です。
J.L.はBiolynx Technology社の株主であります。本研究に関連して、現在本研究に関連する特許出願中のものがあります。著作権情報
Huiru Wang ( wjane60527@yahoo.com )
慧慧バイオファーマ株式会社(Huirui Biopharma, Co.
チーチー・チェン
華安McAbバイオテクノロジー株式会社
Yue Hu
Biolynx Technology (Hangzhou), Co., Ltd.
呉賢村
華安マクブ・バイオテクノロジー株式会社(HuaAn McAb Biotechnology, Co.
リン・ダイ
華安McAbバイオテック株式会社
Yuekai Zhang
バイオリンクステクノロジー(杭州)有限公司(Biolynx Technology (Hangzhou), Co.
Fang Li
華安マクブ・バイオテクノロジー株式会社(HuaAn McAb Biotechnology, Co.
Jinfeng Lu
バイオリンクステクノロジー(杭州)有限公司
Yuxing Chen
華安マクブ・バイオテクノロジー株式会社(HuaAn McAb Biotechnology, Co.
Xiaoling Liu ( liuxl@wizybio.com )
華安McAbバイオテクノロジー株式会社研究論文
キーワード COVID-19感染症、病原体抗体、抗スパイク抗体、新しいメカニズムの病原体
DOI: https://doi.org/10.21203/rs.3.rs-612103/v2
ライセンス:この論文はCreative Commons Attribution 4.0 International Licenseでライセンスされています。COVID-19およびSARS-CoVのスパイクタンパク質によって誘導される病原体抗体ウイルス
Huiru Wang1*, Qiuchi Chen2
Yue Hu3
Xiancong Wu2
Lin Dai2
Yuekai Zhang3
Fang Li2
Jinfeng Lu3
Yuxing
Chen2
およびXiaoling Liu2*が含まれます。
1. Huirui Biopharma, Co., Ltd. 中国、杭州
2. 華安 McAb バイオテクノロジー有限公司 杭州、中国
3. Biolynx Technology (Hangzhou), Co., Ltd. 杭州、中国
Posted at 2021/09/19(Sun) 06:45:05
オカルト・心・科学 | コメント(0) | トラックバック(0) | この記事のURL
この記事のトラックバックURL ->


この記事へのコメント
コメント本文以外は全て入力不要です。